Теоретические основы работы люминесцентных сенсоров. Хронофлуорометры
Ответы
Ответы на вопросы
1. Люминесценция – это избыточное (над тепловым) излучение тел, вызванное каким-либо возбуждающим фактором, которое запаздывает относительно возбуждения на время, значительно больше периода световых колебаний.
2. В зависимости от возбуждающего фактора различают следующие виды люминесценции: фотолюминесценция, которая возникает в результате поглощения возбуждающего света; катодолюминесценция, возникающая в результате бомбардировки быстрыми электронами; рентгенолюминесценция, возникающая в результате возбуждения рентгеновским излучением; хемилюминесценция, возникающая в результате возбуждений при химических реакциях; электролюминесценция, возникающая в результате возбуждения электрическим полем или током и т.д.
3. "Флуоресценция" и "фосфоресценция" различаются временем задержки люминесценции относительно возбуждения. При флуоресценции время задержки очень мало (не больше 1 мс). Она быстро затухает после прекращения возбуждения. При фосфоресценции, наоборот, задержка и затухание люминесценции после прекращения возбуждения очень значительны – больше 1 с.
4. Фотосинтез – это образование углеводов, глюкозы и других органических веществ из молекул воды и углекислого газа в листьях растений под действием солнечного света с выделением кислорода.
5. Фотосинтез является главным источником наращивания биомассы на планете, очищения атмосферы Земли от углекислого газа и обогащения её кислородом. По тому, насколько эффективно происходит в растениях фотосинтез, можно судить об их здоровье и о состоянии окружающей среды, прогнозировать дальнейшее развитие растений и их плодородие. Обнаружив нарушения фотосинтеза, можно еще на ранней стадии выявить заболевания растений, ухудшение состояния окружающей среды и своевременно помочь растениям, проведя соответствующие агротехнические мероприятия (увлажнение, подкормку, обработку против болезней и т.п.).
6. Аббревиатура "ИФХ" обозначает "индукцию флуоресценции хлорофилла" – явление изменения интенсивности флуоресценции хлорофилла по мере развития процесса фотосинтеза при освещении листьев растений после их темновой адаптации. В более широком смысле под этим понимают также и другие изменения интенсивности флуоресценции хлорофилла, вызываемые воздействием внешних факторов.
7. "Кривая ИФХ" – это график зависимости интенсивности флуоресценции хлорофилла от времени, прошедшего после начала освещения листка растения. "Хронофлуорограмма" – это то же самое.
8. "Хронофлуорометр" – это интеллектуальный сенсор для наблюдения индукции флуоресценции хлорофилла и регистрации кривых ИФХ. Хронофлуорометры позволяют на ранней стадии выявлять, отслеживать и документировать изменения в фотосинтетическом аппарате растений.
9. Применение интеллектуальных хронофлуорометров дает следующие преимущества. С помощью встроенного микрокомпьютера можно делать отсчеты интенсивности флуоресценции хлорофилла в любые заданные моменты времени. Хронофлуорометр получается компактным и вполне может использоваться в полевых условиях. В его встроенной памяти можно накапливать множество данных измерений и потом передавать их в сеть связи или в персональный компьютер. Встроенный микрокомпьютер может организовывать сложные эксперименты с модуляцией излучения, включением/выключением дополнительных источников света, изменением температуры листочка и т.д.
10. В качестве примеров эффективного применения хронофлуорометров в растениеводстве можно назвать следующие. Перед весенней обработкой поля гербицидами с помощью хронофлуорометра можно быстро установить, какая дозировка гербицидов является оптимальной для данного конкретного поля. Как правило, это даёт существенную (в среднем двукратную) экономию гербицидов и существенно уменьшает вредное содержание этих веществ в почве, в выращенных на этом поле продуктах, в стекающих с этих полей осадках в реки. С помощью хронофлуорометра можно следить за развитием листьев растений и функционированием их фотосинтетического аппарата. При выявлении отклонений можно своевременно провести необходимые агротехнические мероприятия. Перед обработками против вредителей и болезней растений, стимуляторами роста, подкормками можно определить реально необходимые и допустимые дозировки пестицидов, химреактивов, удобрений. При выращивании растений в теплицах в зимнее время можно оптимизировать реально необходимые затраты на обогрев, освещение, увлажнение и т.д.
11. На американском континенте наиболее популярны сейчас хронофлуорометры марки OS5-FL и OS30 фирмы Opti-Sciences. Первые обеспечивают наиболее широкие возможности, а вторые являются наиболее дешевыми и доступными, имеют малый вес и просты в применении.
12. В Европе чаще всего используются хронофлуорометры марки РАМ-2100 фирмы Heinz Walz.
Ответы к упражнениям
Упражнение 21.1.
Вариант 1. Рентгенолюминесценция, 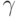 -люминесценция.
-люминесценция.
Вариант 2. Фотолюминесценция.
Вариант 3. Электролюминесценция.
Вариант 4. Биолюминесценция.
Вариант 5. Хемилюминесценция.
Вариант 6. Катодолюминесценция.
Упражнение 21.2.
Вариант 1. "Хлорофилл" – это основной пигмент хлоропластов, имеющихся во всех фотосинтезирующих организмах. Поскольку хлорофилл сильно поглощает сине-голубой, а также красный свет, то листья растений и на отражение, и на просвет выглядят зелеными. Хлорофилл является также и хорошим люминофором. Поэтому, если энергия возбуждения, доставленная к реакционным центрам, не расходуется на фотосинтез, то она излучается хлорофиллом в виде люминесценции. Таким образом, биохимические реакции фотосинтеза и флуоресценция хлорофилла являются конкурирующими каналами утилизации собранной энергии возбуждения. Чем больше поглощенной в хлоропластах световой энергии идет на фотосинтез, тем меньше интенсивность флуоресценции хлорофилла. И, наоборот, если фотосинтез тормозится, угнетается какими-либо факторами, тогда возрастает интенсивность флуоресценции хлорофилла. Таким образом, флуоресценция хлорофилла – это "изобретенный" и предоставленный нам природой механизм сигнализации о ходе фотосинтеза в хлоропласте.
Вариант 2. Интенсивность возбуждающего фотосинтез света принято выражать в "микромолях фотонов на квадратный метр площади за секунду" (мкмольxм–2с–1 или мкмоль/(м2с)). Такая интенсивность означает, что на каждый квадратный метр поверхности каждую секунду падает 1 мкмоль, т.е. 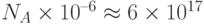 фотонов (
фотонов ( 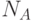 – число Авогадро). Эта единица используется потому, что для фотосинтеза важна не столько суммарная энергия поглощенного света, сколько количество поглощаемых квантов света за единицу времени. Фотосинтез – это квантовый физико-химический процесс. Если принять среднюю энергию фотонов видимого света равной примерно
– число Авогадро). Эта единица используется потому, что для фотосинтеза важна не столько суммарная энергия поглощенного света, сколько количество поглощаемых квантов света за единицу времени. Фотосинтез – это квантовый физико-химический процесс. Если принять среднюю энергию фотонов видимого света равной примерно 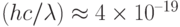 Дж, то интенсивность 1 мкмольxм–2с–1 эквивалентна энергетическому потоку около 240 мВт/м2 или освещенности приблизительно 140 люкс (лк).
Дж, то интенсивность 1 мкмольxм–2с–1 эквивалентна энергетическому потоку около 240 мВт/м2 или освещенности приблизительно 140 люкс (лк).
Вариант 3. "Темновая адаптация" листьев растений состоит в том, что зеленый листок продолжительное время (15?45 мин.) выдерживают в темноте. Она нужна для того, чтобы все запасы возбуждений (активированных молекул и ионов, в том числе ферментов) исчерпались, и фотосинтез полностью прекратился. "Кривую ИФХ" снимают следующим образом. На адаптированный к темноте живой листок начинает действовать свет, и вследствие этого к реакционным центрам стекается поток электронных возбуждений. В начальный момент все каналы фотосинтетического переноса электронов открыты, они максимально интенсивно "откачивают" энергию в цепь реакций фотосинтеза, и флуоресценция хлорофилла минимальна. Её сразу же измеряют. По мере восстановления первичных акцепторов электронов число свободных акцепторов начинает уменьшаться. Откачка электронных возбуждений на фотосинтез замедляется, вследствие чего интенсивность флуоресценции хлорофилла возрастает. Чтобы зафиксировать изменения интенсивности флуоресценции, её измеряют с заданными интервалами времени. В биохимической цепочке фотосинтеза по мере накопления активированных молекул-ферментов предыдущего звена начинают активироваться следующие звенья. Весь фотосинтетический процесс развивается (как бы "разворачивается") во времени. А вместе с ним изменяется во времени и интенсивность флуоресценции хлорофилла, сигнализируя о развитии процесса фотосинтеза. График зависимости интенсивности флуоресценции хлорофилла от времени, начиная от начала освещения, и называют "кривой ИФХ" ("кривой индукции флуоресценции хлорофилла").
Вариант 4. "Быстрой" фазой ИФХ называют интервал времени до выхода интенсивности флуоресценции на максимум. На этом интервале изменения интенсивности флуоресценции происходят быстро (за доли секунды). Участок после выхода на максимум называют "медленной фазой" ИФХ. Она длится десятки и сотни секунд. Характерные точки на кривой ИФХ принято обозначать заглавными латинскими буквами: начальная точка (сразу же после включения освещения) "О"; первые, промежуточные, максимум и минимум "I" и "D", они могут быть плохо выражены; главный максимум "Р"; вторые, промежуточные, минимум и максимум "М" и "S", они тоже могут быть плохо выражены или вообще отсутствовать; установившийся уровень интенсивности "Т".
Характерные значения интенсивности флуоресценции хлорофилла принято обозначать так: 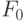 – начальное (наименьшее) значение;
– начальное (наименьшее) значение; 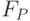 или
или  – значение в максимуме;
– значение в максимуме; 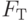 – установившееся значение;
– установившееся значение; 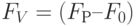 – амплитуда изменения. Значение
– амплитуда изменения. Значение 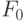 в начальной точке характеризует эффективность собирания света и реакционных центров фотосистемы II. "Быстрая" фаза ИФХ соответствует "световой" стадии фотосинтетического процесса, а "медленная" фаза – "темновой" стадии (разворачивание т.н. "цикла Кальвина") и налаживанию потоков веществ по сосудистой системе листка растения.
в начальной точке характеризует эффективность собирания света и реакционных центров фотосистемы II. "Быстрая" фаза ИФХ соответствует "световой" стадии фотосинтетического процесса, а "медленная" фаза – "темновой" стадии (разворачивание т.н. "цикла Кальвина") и налаживанию потоков веществ по сосудистой системе листка растения.
Вариант 5. Можно назвать следующие примеры влияния внешних факторов на кривую ИФХ. Повышение температуры внешней среды относительно оптимального для данного вида растений значения вызывает уменьшение величины 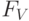 , исчезновение промежуточного пика
, исчезновение промежуточного пика 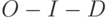 , сокращение времени достижения максимума. При возрастании температуры выше жизненно допустимого уровня (>45-50
, сокращение времени достижения максимума. При возрастании температуры выше жизненно допустимого уровня (>45-50  С) начинает заметно возрастать интенсивность
С) начинает заметно возрастать интенсивность 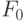 . По этим признакам можно, быстро (еще не выращивая следующее поколение растений) отбирать сорта и экземпляры растений, более стойкие к жаре. Снижение температуры относительно оптимального значения тоже вызывает уменьшение величины
. По этим признакам можно, быстро (еще не выращивая следующее поколение растений) отбирать сорта и экземпляры растений, более стойкие к жаре. Снижение температуры относительно оптимального значения тоже вызывает уменьшение величины 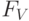 , время достижения максимума растягивается; возрастает отношение
, время достижения максимума растягивается; возрастает отношение 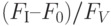 .
При повреждении листвы холодом исчезает
.
При повреждении листвы холодом исчезает 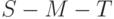 максимум, замедляется
максимум, замедляется  – спад интенсивности флуоресценции. По указанным признакам кривой ИФХ можно быстро отбирать более морозостойкие экземпляры и сорта растений. Засоление почвы приводит к снижению интенсивностей
– спад интенсивности флуоресценции. По указанным признакам кривой ИФХ можно быстро отбирать более морозостойкие экземпляры и сорта растений. Засоление почвы приводит к снижению интенсивностей 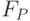 и
и 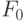 , уменьшается также отношение
, уменьшается также отношение 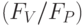 , замедляется
, замедляется  спад интенсивности флуоресценции. По указанным признакам кривой ИФХ можно быстро отбирать растения, более стойкие к засолению почвы. Водный дефицит вызывает уменьшение
спад интенсивности флуоресценции. По указанным признакам кривой ИФХ можно быстро отбирать растения, более стойкие к засолению почвы. Водный дефицит вызывает уменьшение 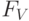 примерно пропорционально уменьшению водного потенциала листьев. Замедляется спад интенсивности флуоресценции на участке
примерно пропорционально уменьшению водного потенциала листьев. Замедляется спад интенсивности флуоресценции на участке 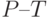 . "Сглаживается" максимум
. "Сглаживается" максимум 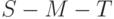 . Совокупность указанных признаков можно использовать для целенаправленного отбора засухоустойчивых сортов и экземпляров растений.
. Совокупность указанных признаков можно использовать для целенаправленного отбора засухоустойчивых сортов и экземпляров растений.
Вариант 6. Кривые ИФХ на всех листьях растения не могут быть совершенно одинаковы. Во-первых, листья сами по себе не одинаковы. Во-вторых, они имеют разный возраст и поэтому содержат разное количество хлорофилла. В-третьих, они растут в разных условиях освещенности, одни – у верхушки растения, другие внутри или внизу в затененных местах. Индивидуальные различия вполне естественны. Для растениеводов важны их усредненные характеристики или характеристики кривых ИФХ, снятых на одних и тех же листьях, но в разное время (на разных стадиях развития, до подкормки и после подкормки и т.д.).
Вариант 7. Собранная и доставленная к реакционным центрам фотосинтеза энергия возбуждения может быть использована: а) на подпитку биохимических реакций фотосинтеза; б) на флуоресцентное излучение хлорофилла в красной области спектра; в) на безизлучательную диссипацию с преобразованием энергии возбуждения в тепловую энергию. Безизлучательная диссипация определяется в основном температурой листьев и мало зависит от эффективности расходования на фотосинтез. А вот фотосинтез и флуоресценция оказываются как бы конкурентами. Чем меньше энергии расходуется на фотосинтез, тем больше излучается в виде флуоресценции. Поэтому по интенсивности флуоресценции и можно судить о текущем отборе энергии на фотосинтез.
Упражнение 21.3.
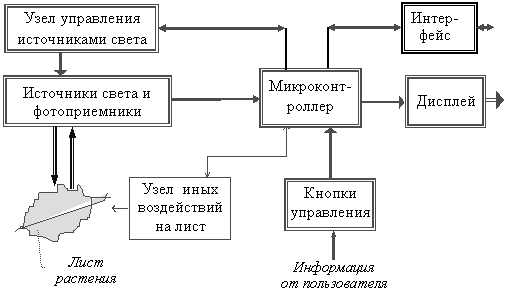
Вариант 1. Общую функциональную схему хронофлуорометра можно представить следующим образом:
Пользователь с помощью кнопок управления выбирает режимы работы, запрашивает и вводит информацию. Микроконтроллер организует работу хронофлуорометра и обрабатывает получаемую информацию. Он, в частности, задает режимы и порядок работы узлу управления источниками света, который обеспечивает нужную последовательность включения и выключения этих источников, интенсивность свечения, их модуляцию. Источники света и фотоприемники располагаются, как правило, в оптоэлектронной головке. Выделенные, усиленные и демодулированные сигналы об интенсивности флуоресценции передаются в микроконтроллер. Обработанные микроконтроллером результаты измерений выводятся для пользователя на дисплей. Накопленные в памяти результаты измерений через интерфейс могут быть переданы в сеть связи или во внешний компьютер. Оттуда же могут быть получены новые микропрограммы работы, новые уставки. В хронофлуорометре могут быть предусмотрены и другие (не световые) воздействия на лист растения: подогрев или охлаждение, увлажнение или, например, вакуумное обезвоживание. Эти воздействия могут также происходить под управлением микроконтроллера в соответствии с заложенной в него микропрограммой исследования. Как легко видеть, хронофлуорометр является активным сенсором, поскольку активно воздействует на объект и наблюдает результаты этого воздействия.
Вариант 2. Для выделения и измерения слабых сигналов флуоресценции хлорофилла на фоне сильного актиничного света, обеспечивающего фотосинтетический процесс, и других световых помех в хронофлуорометрах используется спектральная селекция. Для этого перед фотоприемником (фотоприемниками) устанавливают светофильтр, пропускающий на него свет только в спектральном интервале, соответствующем полосе (полосам) флуоресценции хлорофилла. Свет от всех других источников тщательно отфильтровывают от этих спектральных составляющих. В модулирующих хронофлуорометрах используется дополнительная фильтрация, которую обеспечивает синхронная модуляция/демодуляция измерительного света. При этом обеспечивается весьма высокая избирательность, допускающая работу даже при сильном солнечном освещении.
Вариант 3. Действие большинства применяемых сейчас гербицидов основано на том, что они эффективно угнетают фотосинтетический аппарат растений. Сорняки, прорастающие раньше культурных растений, после обработки гербицидами погибают. А культурные растения, прорастающие позже сорняков, этой участи избегают. Производители гербицидов указывают в своих рекомендациях нормы расхода гербицидов, которые наверняка гарантируют гибель сорняков. Как правило, эти нормы весьма завышены по сравнению с реальной потребностью. С помощью хронофлуорометра можно точно определить, насколько повредился в результате обработки фотосинтетический аппарат сорняков. Благодаря этому, на конкретном поле можно предварительно обработать гербицидами только несколько участков – каждый со своей дозой расхода гербицидов. И уже через несколько часов, необходимых для проникновения гербицидов в листья растений, с помощью хронофлуорометра можно быстро установить, какая дозировка гербицидов является оптимальной для данного конкретного поля. Как правило, это даёт существенную (в среднем двукратную) экономию гербицидов и существенно уменьшает вредное содержание этих веществ в почве, в выращенных на этом поле продуктах, в стекающих с обработанных полей осадках в реки. Такой же принцип – предварительной обработки небольших участков растворами разной концентрации с контролем полученных результатов с помощью хронофлуорометра – можно применить и для оптимизации расхода пестицидов и других реактивов при обработках растений.
Вариант 4. Энергия одного фотона с длиной волны 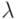 = 470 нм cоставляет
= 470 нм cоставляет 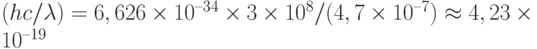 Дж. Тогда квантовая интенсивность 1 мкмольxм–2с–1 эквивалентна энергетическому потоку
Дж. Тогда квантовая интенсивность 1 мкмольxм–2с–1 эквивалентна энергетическому потоку 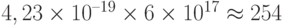 мВт/м2.
мВт/м2.
Вариант 5. При телесном угле выхода излучения 0,46 стерадиана на расстоянии 7 мм световой поток распределяется по площади 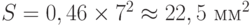 . Следовательно на листок падает энергетический поток
. Следовательно на листок падает энергетический поток 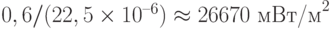 . Учитывая найденную в варианте 4 эквивалентность 1 мкмольxм–2с–1
. Учитывая найденную в варианте 4 эквивалентность 1 мкмольxм–2с–1 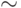 254 мВт/м2, получаем следующую квантовую интенсивность: 26670/254
254 мВт/м2, получаем следующую квантовую интенсивность: 26670/254  105 мкмольxм–2с–1.
105 мкмольxм–2с–1.
Вариант 6. Учитывая найденную в варианте 4 эквивалентность 1 мкмольxм–2с–1 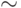 254 мВт/м2, находим, что насыщающая интенсивность света порядка 2000 мкмоль/(м2с) эквивалентна энергетическому потоку 508 Вт/м2. Тогда мощность излучения, падающего на площадь 30 мм2, должна составлять 508x30x10–6 = 1524 мВт. Если всё излучение светодиода попадает на листок, то это и есть требуемая мощность излучения (примерно 1,5 Вт). Если же на листок попадает не весь излучаемый светодиодом свет, то мощность его излучения должна быть соответственно больше.
254 мВт/м2, находим, что насыщающая интенсивность света порядка 2000 мкмоль/(м2с) эквивалентна энергетическому потоку 508 Вт/м2. Тогда мощность излучения, падающего на площадь 30 мм2, должна составлять 508x30x10–6 = 1524 мВт. Если всё излучение светодиода попадает на листок, то это и есть требуемая мощность излучения (примерно 1,5 Вт). Если же на листок попадает не весь излучаемый светодиодом свет, то мощность его излучения должна быть соответственно больше.
Вариант 7. "Хронофлуорометры с модуляцией света" отличаются тем, что, кроме источника непрерывного актиничного освещения, в их состав входят также источник слабого модулированного "измерительного" света и источник, дающий вспышки "насыщающего" света продолжительностью 0,5...2 с с квантовой интенсивностью не менее 2000 мкмоль/(м2с). Модулированный с частотой 2...600 кГц источник света называют "измерительным" потому, что в таком хронофлуорометре выделяют и измеряют только флуоресценцию, синхронно модулированную точно такой же частотой. Квантовая интенсивность "измерительного" пучка света на поверхности листка не должна вызывать существенных изменений состояния фотосинтетических систем, т.е. должна быть намного меньше интенсивности актиничного света. Обычно для измерительного пучка используют интенсивность 0,2...1 мкмоль/(м2с). Благодаря высокоизбирательному синхронному детектированию, удается проводить измерения даже при прямом солнечном освещении. Применение в них "насыщающих" импульсов света приводит к тому, что в течение короткого времени быстро закрываются (насыщаются) практически все каналы оттока электронных возбуждений на фотосинтез. И непосредственно после такой вспышки вся энергия поглощенного света идет только на флуоресценцию или тепловую диссипацию. Интенсивность флуоресценции в этот момент позволяет определить распределение энергии между ними. Дополнительный источник красного света (far-red) в период темновой адаптации способствует эффективному окислению пула пластохинонов, что позволяет корректно определить минимальный сигнал флуоресценции F0.
Вариант 8. Источником действующего света регулируемой интенсивности является в флуорометре OS5-FL твердотельный лазер на длину волны 685 нм. Модулированный "измерительный" свет излучает светодиод с узкополосным светофильтром на 690 нм. При желании можно приобрести также источник модулированного "измерительного" света с длиной волны 450 нм. Импульсы "насыщающего" света регулируемой интенсивности дает 35-ваттная галогенная лампа тоже с узкополосным светофильтром на 690 нм. Для более тщательных опытов имеется также источник далекого красного (far-red) света с фильтром на 735 нм. В период темновой адаптации такое облучение способствует эффективному окислению пула пластохинонов, что позволяет корректно определить минимальный сигнал флуоресценции 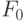 . Перед
. Перед 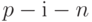 фотодиодом, который воспринимает флуоресценцию хлорофилла, установлен светофильтр, пропускающий лишь спектральную полосу от 700 до 750 нм.
Частота модуляции может программно изменяться в ходе работы от 250 Гц до 40 кГц. Измерение интенсивности флуоресценции может осуществляться с интервалами времени от 0,2 мс до 2 с, которые тоже задаются программно. Продолжительность записи хронофлуорограмм – от 2 секунд до 45 мин. (по желанию – до 16 ч.). Объем памяти данных – 512 кбайт. Сенсор имеет ЖК дисплей 320x240 пикселей с подсветкой и 9 клавиш для взаимодействия с пользователем. В сенсор встроен источник автономного питания – аккумуляторная батарея на 12 В / 3,4 А-ч и привод 3,5-дюймовой дискеты, на которую можно переписывать полученные данные. Имеется внешний интерфейс RS-232. Размеры этого интеллектуального сенсора довольно значительны 280x180x130 мм, масса – 5 кг. Тем не менее, его относят к группе портативных. К сенсору можно приобрести такие аксессуары, как специальные кюветы для темновой адаптации, термостабилизации и для опытов с изменением температуры, кюветы для работы с водорослями и другие.
фотодиодом, который воспринимает флуоресценцию хлорофилла, установлен светофильтр, пропускающий лишь спектральную полосу от 700 до 750 нм.
Частота модуляции может программно изменяться в ходе работы от 250 Гц до 40 кГц. Измерение интенсивности флуоресценции может осуществляться с интервалами времени от 0,2 мс до 2 с, которые тоже задаются программно. Продолжительность записи хронофлуорограмм – от 2 секунд до 45 мин. (по желанию – до 16 ч.). Объем памяти данных – 512 кбайт. Сенсор имеет ЖК дисплей 320x240 пикселей с подсветкой и 9 клавиш для взаимодействия с пользователем. В сенсор встроен источник автономного питания – аккумуляторная батарея на 12 В / 3,4 А-ч и привод 3,5-дюймовой дискеты, на которую можно переписывать полученные данные. Имеется внешний интерфейс RS-232. Размеры этого интеллектуального сенсора довольно значительны 280x180x130 мм, масса – 5 кг. Тем не менее, его относят к группе портативных. К сенсору можно приобрести такие аксессуары, как специальные кюветы для темновой адаптации, термостабилизации и для опытов с изменением температуры, кюветы для работы с водорослями и другие.
Вариант 9. Хронофлуорометр РАМ-2100 фирмы Heinz Walz с основным блоком размерами 240x105x110 мм является хронофлуорометром с модуляцией света. В качестве источников действующего и насыщающего света служат в нём матрицы светодиодов с длиной волны 655 нм и 735 нм (последние – для возбуждения фотосистем І) и миниатюрная галогенная лампа белого света. Эти источники света крепятся на специальной подставке. Измерительный модулированный свет излучается светодиодами на длине волны 655 нм в виде импульсов продолжительностью 3 мкс с частотой 600 Гц или 20 кГц. В памяти программ сенсора записаны программы стандартных экспериментов по индукции флуоресценции хлорофилла. Предусмотрена возможность для пользователей программировать свои варианты экспериментов, которые автоматически будет выполнять микропроцессор после нажатия клавиши "Пуск". В хронофлуорометре имеются графический дисплей, клавиатура управления и внешний интерфейс RS-232.