|
Подскажите пожалуйста а как можно посмотреть на сколько балов сдал экзамен? Я не сфоткал на какой бал написал экзамен. Думал на сертификате будет написанно на сколько сдал написанно. |
Неинвазивные глюкометры. Спектрофотометрический сенсор хлорофилла
Цель лекции: oзнакомить слушателей не только с успешными разработками интеллектуальных сенсоров, но и с некоторыми не удавшимися пока проектами создания неинвазивных спектрофотометрических глюкометров. Раскрыть причины неудач. На примере сенсора хлорофилла показать, как благодаря изобретательности иногда можно обходить, казалось бы, непреодолимые трудности в применении спектрофотометрического метода
20.1. Неинвазивные глюкометры
Глюкометрами сокращенно называют интеллектуальные сенсоры для измерения содержания глюкозы в крови человека. Иногда их называют также "приборами для измерения сахара крови". Остановимся вкратце на важности создания таких сенсоров.
Известно, что регулирование концентрации глюкозы в крови (КГК) является одним из жизненно важных процессов саморегулирования человеческого организма. В норме КГК поддерживается в пределах от 60 до 100 мг% (от 3,3 до 5,5 ммоль/л). В этих пределах обеспечивается оптимальная жизнедеятельность клеток и органов, особенно нервных клеток и мозга человека. Глюкоза является для клеток источником жизненной энергии и исходным материалом для многих биохимических синтезов. Как уже отмечалось в лекции 17, сейчас в мире до 200 млн. людей больны диабетом. Эта болезнь на сегодня, к сожалению, считается неизлечимой и сопровождает человека всю жизнь. Во избежание тяжелых осложнений заболевшие диабетом люди вынуждены придерживаться специального режима жизни и питания и периодически брать пробы своей крови "на сахар". Поэтому еще в 70-х гг. ХХ в., когда стало ясно, что диабет является массовым заболеванием, начались интенсивные разработки неинвазивных методов измерения КГК [ [ 190 ] ] для того, чтобы избавить людей от необходимости частого травмирования тела. Конгресс США, а за ним правительства и некоторых других стран выделили на эти разработки значительные средства. Тем не менее, задача оказалась трудноразрешимой.
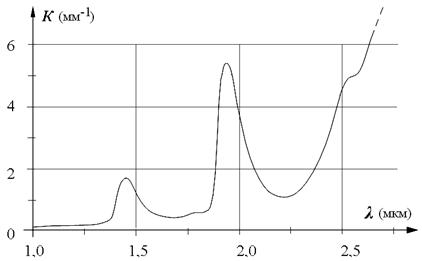
В 80-90 годы ХХ в. наибольшие надежды возлагались именно на спектрофотометрические методы. С самого начала было ясно, что видимая область спектра не подходит для этих измерений, поскольку глюкоза здесь прозрачна, т.е. практически не поглощает свет. Поэтому усилия были направлены на создание неинвазивного спектрофотометрического глюкометра в инфракрасной (ИК) области спектра [ [ 18 ] , [ 52 ] , [ 53 ] , [ 59 ] , [ 65 ] , [ 82 ] , [ 96 ] , [ 98 ] , [ 100 ] , [ 114 ] , [ 140 ] , [ 163 ] , [ 284 ] ]. Главным препятствием в этой области оказалась всегда присутствующая в биологической ткани в большом количестве вода, которая сильно поглощает инфракрасный свет. Тем не менее, она имеет здесь (см. рис. 20.1) несколько спектральных "окон прозрачности" в диапазонах длин волны до 1,35 мкм, от 1,55 до 1,85 мкм и от 2,1 до 2,3 мкм.
При длине волны 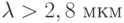 коэффициент поглощения воды превышает уже 6 мм–1, т.е. на каждом миллиметре пути только за счет поглощения молекулами воды такой ИК свет ослабляется в
коэффициент поглощения воды превышает уже 6 мм–1, т.е. на каждом миллиметре пути только за счет поглощения молекулами воды такой ИК свет ослабляется в  .
.
20.1.1. Первые спектрофотометрические глюкометры фирмы Futrex
Одними из первых на разработку промышленного неинвазивного спектрофотометрического глюкометра отважились R. Rosenthal и его фирма Futrex Inc. (США) [ [ 100 ] , [ 114 ] ]. Для измерений они просвечивали светом с непрерывным спектром палец руки. Свет, прошедший сквозь палец, разлагался в спектр, и измерялись спектральные интенсивности этого света на нескольких длинах волны. В БИК области до 1,8 мкм были отобраны спектральные интервалы, характерные для поглощения света глюкозой и для поглощения другими, "фоновыми" веществами тела (вода, жиры, гемоглобин и другие белки). Для расчета концентрации глюкозы применялись методики многоволновой спектрофотометрии, чтобы можно было выделить вклад и определить относительно небольшую концентрацию именно глюкозы. Разработчикам удалось улавливать и измерять малые концентрации глюкозы на уровне 100 мг% в кюветах с калиброванными растворами глюкозы и фоновых веществ. Был создан и выпущен во многих экземплярах для испытаний экспериментальный образец неинвазивного ИК глюкометра, внешний вид которого показан на рис. 20.2.

Рис. 20.2. Вид прибора "Dreem Beam" для неинвазивного измерения сахара крови, разработанного фирмой Futrex
Однако при испытаниях на реальных объектах – пальцах человека – все оказалось намного хуже. Разработчики не учли то, что кровь в тканях пальца занимает лишь 1-5 % объема, т.е. средняя концентрация глюкозы в ткани пальца составляет не 100 мг %, как в крови, а в 20–100 раз меньше. Количество молекул глюкозы на пути света в человеческом теле почти на 4 порядка меньше, чем количество молекул воды, и на 2 порядка меньше, чем количество молекул гемоглобина. Это обстоятельство, а также непонимание разработчиками проблемы корректного пересчета измеряемой концентрации глюкозы в тканях на КГК помешали доведению разработки неинвазивного глюкометра до промышленных образцов.
20.1.2. Другие попытки создания спектрофотометрического глюкометра
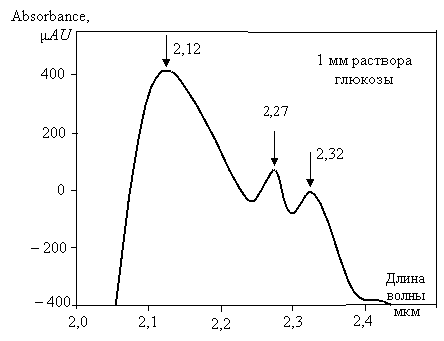
J.T. Olеsberg из университета штата Айова вместе со своими сотрудниками надеялся достичь успеха, работая в третьем "окне прозрачности" воды, т.е. в диапазоне длин волны от 2 до 2,5 мкм [ [ 96 ] ], где имеются три характерных пика поглощения глюкозы, показанных на рис. 20.3. Вдоль горизонтали здесь отложена длина волны в мкм, а по вертикали – разность оптических плотностей 1 мм слоя раствора глюкозы и чистой воды
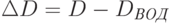 |
( 20.1) |
Т.е. это – т.н. "дифференциальный спектр поглощения глюкозы". Вертикальная шкала (Аbsorbance) проградуирована в единицах оптической плотности 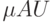 . Напомним, что 1
. Напомним, что 1 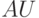 ( A bsorpbance U nity) – это оптическая плотность такого слоя, при которой десятичный логарифм пропускания слоя
( A bsorpbance U nity) – это оптическая плотность такого слоя, при которой десятичный логарифм пропускания слоя  , т.е. свет ослабляется таким слоем в 10 раз. Единица
, т.е. свет ослабляется таким слоем в 10 раз. Единица 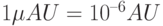 . При тех длинах волны, при которых раствор глюкозы поглощает свет сильней, чем вода,
. При тех длинах волны, при которых раствор глюкозы поглощает свет сильней, чем вода, 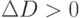 . А там, где поглощение раствора глюкозы слабей, чем поглощение чистой воды, имеем
. А там, где поглощение раствора глюкозы слабей, чем поглощение чистой воды, имеем 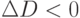 .
.
На
рис.
20.3 стрелками указаны 3 максимума поглощения. В наибольшем из них (на длине волны 2,12 мкм) 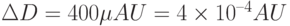 . Поскольку
. Поскольку 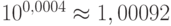 , то пропускание 1 мм слоя 5-милимолярного раствора глюкозы примерно лишь на 0,1 % больше пропускания чистой воды. И все же, используя специальные алгоритмы (partial least squаres regression) для выделения вклада в эти спектры именно глюкозы, разработчикам удалось измерять концентрацию глюкозы в модельных растворах глюкозы с разными фоновыми веществами. Хотя вода в этом окне прозрачности уже довольно сильно поглощает (слой воды толщиной 1 мм ослабляет свет в 40-50 раз), разработчики преодолели это препятствие, используя новейший БИК полупроводниковый лазер, разработанный в Fraunhofer-Instituts fur Angewandte Festkorperphysik (Freiburg, ФРГ: http://www.iaf.fraunhofer.de), способный изменять длину волны излучения.
Изучение публикаций разработчиков показало, что и они недостаточно понимали разницу между концентрацией глюкозы в крови человека и измеряемой спектрофотометрическим методом средней концентрацией глюкозы в участке тела, который просвечивается светом. Пока что никаких сообщений разработчиков об испытаниях созданного сенсора на реальных объектах, к сожалению, нет.
, то пропускание 1 мм слоя 5-милимолярного раствора глюкозы примерно лишь на 0,1 % больше пропускания чистой воды. И все же, используя специальные алгоритмы (partial least squаres regression) для выделения вклада в эти спектры именно глюкозы, разработчикам удалось измерять концентрацию глюкозы в модельных растворах глюкозы с разными фоновыми веществами. Хотя вода в этом окне прозрачности уже довольно сильно поглощает (слой воды толщиной 1 мм ослабляет свет в 40-50 раз), разработчики преодолели это препятствие, используя новейший БИК полупроводниковый лазер, разработанный в Fraunhofer-Instituts fur Angewandte Festkorperphysik (Freiburg, ФРГ: http://www.iaf.fraunhofer.de), способный изменять длину волны излучения.
Изучение публикаций разработчиков показало, что и они недостаточно понимали разницу между концентрацией глюкозы в крови человека и измеряемой спектрофотометрическим методом средней концентрацией глюкозы в участке тела, который просвечивается светом. Пока что никаких сообщений разработчиков об испытаниях созданного сенсора на реальных объектах, к сожалению, нет.
Приблизительно такие же результаты для указанного участка спектра поглощения глюкозы приведены и в работе [ [ 163 ] ]. Авторы этой работы и патентной заявки [282] тоже надеялись достичь успеха, используя дифференциальные спектры поглощения БИК света. Для быстрого получения спектра пропускания в работе [ [ 282 ] ] использовался перенастраиваемый акустооптический осцилляторный фильтр (acousto-optic variable oscillation tunable filter), о котором мы уже кратко рассказали в "Спектрофотометрические сенсоры как один из видов оптических сенсоров. Фотоплетизмографы. Оксиметры и пульсоксиметры" . Это позволило использовать весь арсенал непрерывных методов селекции слабого сигнала глюкозы. Но о решающих успехах на реальных объектах и эти разработчики тоже пока и не сообщали.
Фирмы Foviopitics Inc. (Lexington, Kentucky, США: Интернет-страницы http://www.fovioptics.com/ и http://www.3rddimensiondesign.com/vonallmen/companies/FoviOptics.pdf) и Visionary Medical Products Corporation (Reno, Nevada: http://www.vmpc.com) сообщили о проводимой ими разработке неинвазивного спектрофотометрического сенсора глюкозы, использующего "естественное окно для доступа света к крови" – человеческий глаз. Речь идет о зондировании светом определенных длин волны, об измерении и анализе спектральных интенсивностей света, отраженного от богатой кровеносными сосудами сетчатки глаза. Методы расчета концентрации глюкозы в крови на основе анализа отраженного света пока не раскрывались, так как являются предметом патентования.
Фирма Infratec Inc. (Wilton, Connecticut, США) разрабатывает спектрофотометрический сенсор глюкозы, в котором для измерений используется не внешний свет, а собственное инфракрасное тепловое излучение самих биологических тканей. В области длин волны от 8 до 14 мкм (средняя ИК область спектра) были выявлены характерные полосы теплового излучения глюкозы при 9,6 мкм и 10,9 мкм. Используя методы и достижения термоэмиссионной спектрофотометрии [ [ 34 ] , [ 81 ] ] и возможности микроминиатюризации, разработчикам удалось вместить чувствительную часть прибора в габариты крохотной капсулы. Ее вставляют пациенту в слуховой канал уха и измеряют тепловое излучение на указанных длинах волны от барабанной перепонки, которая давно считается одной из наиболее термостабильных частей человеческого тела. Сообщено, что предварительные медицинские испытания показали возможность измерять КГК в диапазоне от 30 до 300 мг % с относительной погрешностью примерно 12 %.
20.1.3. Окклюзионный спектрофотометрический глюкометр
Обнадёживающий способ неинвазивного измерения КГК спектрофотометрическим методом предложен в [ [ 276 ] ]. Один из возможных вариантов реализации этого способа показан на рис. 20.4. При подготовке к измерению пациент вставляет конечную фалангу своего пальца 2 сквозь кольцо-манжету 11 и кладет пучку пальца на измерительное ложе 1. Поверхность пальца автоматически входит в оптический контакт с выведенными в это ложе волоконно-оптическими световодами 17-19.
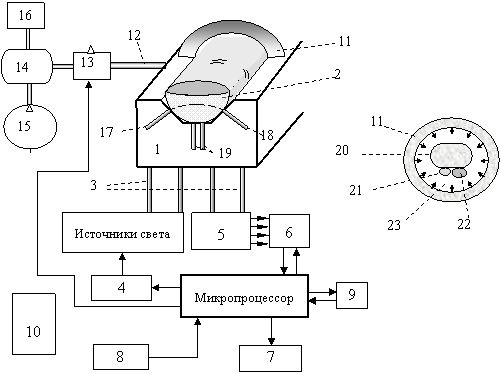
Рис. 20.4. Функциональная схема окклюзионного спектрофотометрического неинвазивного глюкометра: 1 – измерительное ложе для пальца; 2 – передняя фаланга пальца; 3 – оптические связи; 4 – модулятор источников света; 5 – фотоприемники и усилители сигналов; 6 – демодулятор и АЦП; 7 – дисплей; 8 – клавиатура управления; 9 – интерфейс с внешним компьютером; 10 – блок питания; 11 – надувное кольцо-манжета; 12 – соединитель; 13 – управляемый 2-ходовой вентиль; 14 – ресивер; 15 – нагнетатель воздуха; 16 – манометр; 17-19 – волоконно-оптические световоды. Справа – кольцо-манжета 11 и сжимаемый палец в условном сечении: 20 – костная ткань; 21 и 22 – артериальные и венозные сосуды; 23 – мягкие ткани
Перед измерениями с помощью компрессора 15 (это может быть и обычная резиновая "груша") в ресивер 14 нагнетается воздух до достижения заданного давления (например, 50-60 мм рт. ст.), которое контролируется манометром 16. Трёхходовой вентиль 13 сначала пневматически соединяет надувное эластичное кольцо-манжету 11 с атмосферой, и на первом этапе измерений дополнительного давления в ней нет.
После нажатия кнопки "Пуск" на клавиатуре 8 микропроцессор через схему управления светодиодами 4 включает источник света с длиной волны 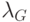 , характерной для поглощения глюкозой, и по заранее заданной программе модулирует его интенсивность, одновременно управляя синхронной демодуляцией соответствующего светового сигнала в узле 5. Модулированный свет через волоконно-оптический световод 17 поступает к пучке пальца 2 и входит перпендикулярно к его поверхности в мягкие ткани пальца в виде остро направленного светового зонда. Часть света от этого зонда, рассеиваясь вблизи наиболее вероятной траектории, условно изображенной на рисунке штриховой линией, проходит сквозь ткани пальца и попадает в приемный световод 18.
Вдоль соответствующего оптического волокна выделенный световой сигнал передается к фотоприемнику 5, превращается в электрический сигнал, усиливается, демодулируется и в узле 6 превращается в двоичный код измеренной спектральной интенсивности. В микропроцессоре этот двоичный код (
, характерной для поглощения глюкозой, и по заранее заданной программе модулирует его интенсивность, одновременно управляя синхронной демодуляцией соответствующего светового сигнала в узле 5. Модулированный свет через волоконно-оптический световод 17 поступает к пучке пальца 2 и входит перпендикулярно к его поверхности в мягкие ткани пальца в виде остро направленного светового зонда. Часть света от этого зонда, рассеиваясь вблизи наиболее вероятной траектории, условно изображенной на рисунке штриховой линией, проходит сквозь ткани пальца и попадает в приемный световод 18.
Вдоль соответствующего оптического волокна выделенный световой сигнал передается к фотоприемнику 5, превращается в электрический сигнал, усиливается, демодулируется и в узле 6 превращается в двоичный код измеренной спектральной интенсивности. В микропроцессоре этот двоичный код ( 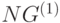 ) запоминается.
) запоминается.
Дальше микропроцессор через схему управления 4 выключает первый и включает второй источник света с длиной волны 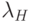 , характерной для поглощения гемоглобином. Модулированный свет от этого второго источника через волоконно-оптический световод 19 передается к пальцу. И, аналогично описанному выше, осуществляется измерение второй спектральной интенсивности и запоминается ее двоичный код
, характерной для поглощения гемоглобином. Модулированный свет от этого второго источника через волоконно-оптический световод 19 передается к пальцу. И, аналогично описанному выше, осуществляется измерение второй спектральной интенсивности и запоминается ее двоичный код 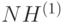 .
.
После этого по сигналу от микропроцессора вентиль 13 перекрывает выход кольца-манжеты 11 в атмосферу и присоединяет его к ресиверу 14. Поскольку объем ресивера во многие десятки раз больше внутреннего объема кольца-манжеты, то давление в манжете 11 быстро возрастает до заданного уровня. Она, в свою очередь, создает такое же давление на ткани пальца. На рис. 20.4 справа это схематически показано стрелками. Через мягкую ткань пальца 23 давление передается на костные ткани 20 и на артериальные (21) и венозные (22) кровеносные сосуды. Давление в ресивере выбрано так, чтобы давление в артериальных сосудах оставалось выше, чем давление извне. Благодаря этому, кровь продолжает поступать в палец. А давление внутри венозных сосудов оказывается ниже давления извне, поэтому вены перекрываются, и отток крови из пальца прекращается. Конечная фаланга пальца дополнительно наполняется кровью до тех пор, пока давление внутри вен не сравняется с внешним давлением манжеты.
Для слежения за кровенаполнением пальца микропроцессор организует периодическое измерение спектральной интенсивности на длине волны 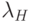 . Когда значение этой спектральной интенсивности стабилизируется (это означает стабилизацию после достижения нового уровня кровенаполнения), микропроцессор запоминает соответствующий код
. Когда значение этой спектральной интенсивности стабилизируется (это означает стабилизацию после достижения нового уровня кровенаполнения), микропроцессор запоминает соответствующий код 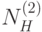 . Затем производится измерение спектральной интенсивности на длине волны
. Затем производится измерение спектральной интенсивности на длине волны 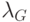 при новом уровне кровенаполнения и запоминается соответствующее значение
при новом уровне кровенаполнения и запоминается соответствующее значение  . После окончания измерений микропроцессор подает сигнал на управляемый вентиль 13, который перекрывает выход кольца-манжеты 11 к ресиверу 14 и открывает выход в атмосферу. Давление в манжете снижается и уравнивается с атмосферным. Теперь пациент может свободно вынуть палец из измерительного пальцевого ложа. Микропроцессор рассчитывает концентрацию глюкозы в крови пациента и высвечивает полученное значение на дисплее 7.
. После окончания измерений микропроцессор подает сигнал на управляемый вентиль 13, который перекрывает выход кольца-манжеты 11 к ресиверу 14 и открывает выход в атмосферу. Давление в манжете снижается и уравнивается с атмосферным. Теперь пациент может свободно вынуть палец из измерительного пальцевого ложа. Микропроцессор рассчитывает концентрацию глюкозы в крови пациента и высвечивает полученное значение на дисплее 7.