|
Подскажите пожалуйста а как можно посмотреть на сколько балов сдал экзамен? Я не сфоткал на какой бал написал экзамен. Думал на сертификате будет написанно на сколько сдал написанно. |
Принципы работы электрохимических сенсоров. Потенциометрические сенсоры
Цель лекции: разъяснить основные понятия: "электрохимический элемент", "полуэлемент", "гальванический электрод", "электродный потенциал", "ионоселективный электрод". Объяснить, почему электрохимический элемент может быть использован в качестве сенсора. Обосновать классификацию электрохимических сенсоров. Ознакомить с методами обеспечения и повышения их селективности. Рассказать о принципе определения концентрации ионов аналита с помощью концентрационной ячейки и уравнения Нернста, о промышленно выпускаемых ионоселективных электродах и потенциометрических сенсорах, их возможностях. Указать на роль микропроцессора в составе интеллектуальных потенциометрических сенсоров. Объяснить принцип действия потенциометрических биосенсоров.
15.1. Принцип работы электрохимического элемента
Электрохимические сенсоры являются, строго говоря, одним из видов электрических сенсоров. Но электрические сигналы возникают здесь в склонной к химическим превращениям системе "электронный проводник - электролит" и являются настолько специфическими, что их обычно выделяют (особенно химики) в отдельный класс сенсоров.
Когда электронный проводник тока (металл, графит, электронный полупроводник) контактирует с ионным проводником (ионным раствором, расплавом, гелем, сгущенным или твердым электролитом) и является относительно него химически активным, то в местах контакта происходит химическая реакция окисления металла, в ходе которой часть электронов переходит из металла в электролит ( рис. 15.1, а ).
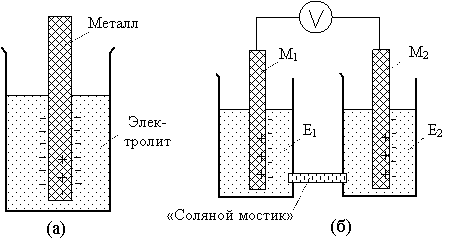
Рис. 15.1. а) Электронный проводник тока в контакте с электролитом ("полуэлемент"); б) электрохимический элемент: два электрически соединенных полуэлемента
Примеры таких химических реакций:
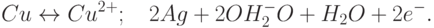 |
( 15.1) |
Вследствие этого металл заряжается положительно, а электролит – отрицательно, так что между металлом и электролитом возникает разность потенциалов. Если электрическая цепь разомкнута, и постоянный электрический ток протекать через систему не может, то довольно быстро устанавливается динамическое равновесие: число электронов, которые переходят из металла в электролит за единицу времени в результате прямой химической электродной реакции, сравнивается с числом электронов, которые переходят из электролита в металл под действием разности потенциалов. При этом протекает обратная химическая электродная реакция. Разницу потенциалов, которая устанавливается при достижении динамического равновесия, называют электродным потенциалом [ [ 206 ] ].
Равновесие и, следовательно, значение электродного потенциала зависят от всех факторов, которые могут повлиять на кинетику прямой и обратной электродной химической реакции:
- от энергии активации этой реакции;
- от материала, из которого сделан электронный проводник;
- от состава и концентрации тех ионов в электролите, которые могут вступать в окислительно-восстановительные реакции;
- от природы этих ионов, от их подвижности;
- от температуры электролита и электрода;
- от условий диффузии и перемешивания;
- от наличия источников и стоков участвующих веществ, напр., от притока веществ извне или выпадения продуктов реакции в осадок и т.д.
Электронный проводник может быть жидким, – например, жидкая ртуть.
Электронный проводник может быть даже химически инертным. Важно то, что он становится источником или стоком электронов и создает поверхность, на которой оказываются возможны окислительно-восстановительные химические реакции между компонентами, присутствующими в самом электролите. Например, такие реакции:
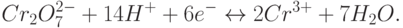 |
( 15.2) |
Электродная реакция может происходить также между компонентами электролита и веществом, которое каким-то образом непрерывно доставляется к поверхности электронного проводника из стороннего источника. Известным примером является так называемый " водородный электрод ". Электронным проводником тока в нём служит платиновая проволока, часть которой находится в трубке, заполненной водородом. Водород, хорошо растворяясь в платине, диффундирует вдоль проволоки и в местах контакта с электролитом может выходить наружу. Тогда на поверхности платины может протекать химическая реакция
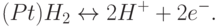 |
( 15.3) |
Электронный проводник в контакте с ионным проводником, если на границе их раздела могут происходить окислительные или окислительно-восстановительные химические реакции, называют гальваническим электродом .
Гальванический электрод часто используют как элемент сенсоров, чувствительных к любому из факторов, существенно влияющих на величину электродного потенциала.
В качестве химически активных электронных проводников чаще всего применяют  , а в качестве химически инертных –
, а в качестве химически инертных – 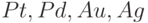 , графит.
, графит.
Электродный потенциал отдельного гальванического электрода нельзя измерить непосредственно. Но можно измерять разность потенциалов между двумя или несколькими последовательно соединенными гальваническими электродами. Систему из двух электрически соединенных навстречу друг другу гальванических электродов ( рис. 15.1, б ) называют электрохимическим элементом (или электрохимической ячейкой ), а каждую из двух составляющих его частей называют также полуэлементами.
В электрохимическом элементе, чтобы реализовать встречное включение полуэлементов, электрически соединяют между собой электролиты Е1 и Е2. Соединение это должно обеспечивать возможность протекания электрического тока, но препятствовать смешиванию электролитов. Другими словами, оно должно обеспечивать возможность переноса электрических зарядов (электронов и некоторых ионов), но препятствовать переносу большинства других ионов, особенно ионов аналита, т.е. ионов, концентрацию которых надо определить. Таким соединением может быть, например, пористая глиняная перегородка, через которую проникают электроны, но не проникает большинство ионов; могут быть стеклянная или полимерная мембрана, "соляной мостик".
Разность потенциалов между электродами М1 и М2 надо измерять очень высокоомным вольтметром, так чтобы протеканием электрического тока через него и смещением из-за этого равновесия электродных химических реакций можно было пренебречь.
