| Россия |
Медицинская нейроинформатика
Экспертные системы, созданные на основе нейросетевой технологии группой "НейроКомп"
Создание каждой ЭС проводилось согласно разработанной технологии и включало: изучение проблемы; постановку задачи; набор обучающих данных и тестирующих примеров; обучение нейросетей; определение оптимальной схемы ЭС ; проведение дополнительных экспериментов; разработку и создание интерфейса программы; подключение к ней обученных нейросетей; испытание системы на примерах, не входящих в обучающую выборку; доучивание системы на этих примерах.
Прогнозирование осложнений инфаркта миокарда.
Поиски возможностей прогнозирования осложнений, которые могут возникнуть в госпитальный период инфаркта миокарда, очень актуальны и являются одной из наиболее сложных задач кардиологии. Прогнозирование необходимо осуществлять при поступлении больного в стационар, сразу же после проведения стандартных методов обследования. Оно должно быть быстрым, проводиться неоднократно в процессе наблюдения за больным по мере поступления новых данных о его состоянии.
Получение прогноза осложнений позволяет врачу целенаправленно проводить профилактику, усилить наблюдение за больным, скорректировать режим физической активности пациента (особенно в предполагаемые сроки возникновения осложнения). Прогноз может определять более длительное и интенсивное лечение антикоагулянтами при угрозе тромбоэмболических осложнений, антиаритмическими препаратами - для профилактики аритмий.
При создании базового ядра ЭС прогнозирования осложнений инфаркта миокарда выбрано 4 вида осложнений, достаточно частых и/или довольно опасных [5.49]. Это фибрилляция предсердий, тромбоэмболические осложнения, перикардит и возникновение/усугубление хронической СН. При постановке задачи мы исходили из необходимости прогнозировать возможность возникновения каждого из четырех выбранных осложнений в отдельности и возможного срока его появления, считая от момента поступления больного в стационар. Таким образом, задача разбивается на 8 подзадач, четыре из которых решаются нейросетями-классификаторами (возникновение осложнений), и четыре - нейросетями-предикторами (сроки возникновения осложнений).
Были выбраны 32 обучающих параметра, отражающие клиническое состояние больного инфарктом миокарда на момент поступления в клинику, данные анамнеза и результаты лабораторных и функциональных исследований: возраст, пол, глубина и локализация инфаркта (по данным электрокардиографии), количество инфарктов в анамнезе, характеристика предшествующей стенокардии, наличие и тяжесть гипертонической болезни и сердечной недостаточности, наличие в анамнезе нарушений сердечного ритма и проводимости, эндокринных заболеваний, тромбоэмболий, хронического бронхита, концентрация калия и натрия в крови, частота сердечных сокращений, характеристика выбранных показателей ЭКГ, размеры отделов сердца по данным эхокардиографии.
Исследованы 300 клинических примеров ( таблица 5.4). Для экспериментов из общей выборки отдельно для каждого типа нейросетей были выделены обучающая группа ( 250 человек) и контрольная (тестирующая) группа ( 50 человек). Разделение выборки производилось случайным образом. Для прогнозирования возникновения каждого осложнения создавались несколько нейросетей, составляющих консилиум. Все нейросети вначале обучались на 250 пациентах обучающей выборки, а затем тестировались на контрольной группе. Результаты теста определялись голосованием в каждом консилиуме. Результаты теста контрольной выборки для прогнозирования фибрилляции предсердий приведены в таблица 5.5.
| Осложнение | Количество больных | |
|---|---|---|
| Фибрилляция предсердий | нет пароксизмальная форма постоянная форма |
217 60 23 |
| Перикардит | нет есть |
172 128 |
| Тромбоэмболические осложнения | нет есть |
242 58 |
| Возникновение или усугубление сердечной недостаточности | нет есть |
144 156 |
| Известный класс | Вычислено как... | ||
|---|---|---|---|
| Класс 1 | Класс 2 | Класс 3 | |
|
Нет ФП - 30 примеров |
28 | 2 | - |
|
Пароксизмальная форма ФП - 12 примеров |
- | 11 | 1 |
|
Постоянная форма ФП - 8 примеров |
- | 1 | 7 |
Процент правильно распознанных примеров в тестирующей выборке при прогнозировании возникновения перикардита составил 76%, тромбоэмболий - 82%, возникновения/усугубления сердечной недостаточности - 78%.
Отдельно были созданы и обучены нейросети-предикторы для прогноза сроков возникновения осложнений (начиная с момента поступления больного в клинику).
Система назначения оптимальной стратегии лечения больных облитерирующим тромбангиитом и прогнозирования его непосредственных исходов.
Облитерирующий тромбангиит (болезнь Бюргера) - тяжелое воспалительное заболевание сосудов мелкого и среднего калибра, сопровождающееся тромбозом и нарушением их проходимости. Этиология этого заболевания до настоящего времени остается неизвестной. Подавляющее большинство больных тромбангиитом - мужчины молодого возраста ( 18 - 45 лет).
Лечение облитерирующего тромбангиита - трудная, далеко еще не решенная задача. В начальных стадиях заболевания обычно ограничиваются терапевтическими мероприятиями - назначением дезагрегантов, противовоспалительных и антигистаминных препаратов. Однако заболевание часто носит злокачественный характер и быстро приводит к ампутации конечности.
В 1990 - 1994 гг. в отделении хирургии сосудов Краевой Клинической Больницы № 1 г. Красноярска под наблюдением находилось 130 больных облитерирующим тромбангиитом. На каждого больного заполнялась анкета, состоящая из 3 разделов.
Первый раздел ( 104 пункта) включает вопросы, касающиеся анамнеза жизни и данного заболевания, сопутствующих заболеваний; состояние органов и систем, подробное описание имеющегося у больного тромбангиита с характеристикой состояния сосудов конечностей, данные лабораторных и инструментальных методов исследования, характеристику проводившегося ранее лечения. Другими словами, этот раздел отражает исходный статус больного на момент его поступления в стационар.
Второй раздел ( 11 пунктов) характеризует проведенное в стационаре лечение (консервативное и/или оперативное).
Третий раздел ( 4 пункта) содержит сведения о непоcредственных исходах проведенного лечения.
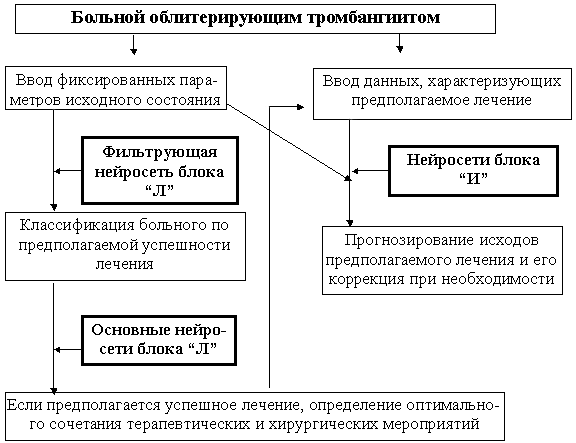
Существующие методы лечения тромбангиита часто малоэффективны и процент выполняемых ампутаций остается высоким. Перед врачом стоит задача подобрать оптимальное сочетание методов лечения, действующих на ведущие звенья патогенеза у конкретного больного. Целью проводимого исследования стало создание нейросетевой ЭС для прогноза непосредственных исходов заболевания и выбора оптимального сочетания терапевтических и хирургических воздействий. Соответственно этому ЭС подразделяется на два функциональных блока, каждый из которых решает свой круг задач [5.50].
Один блок (блок " И " - исходы) прогнозирует непосредственные исходы заболевания, которые зависят от двух групп параметров. Первая группа - исходный статус больного, фиксированные параметры, отражающие состояние больного на момент поступления в клинику, а также данные анамнеза. Однако исход заболевания зависит не только от исходных параметров, но и от проводимого в клинике лечения. Поэтому вторая группа параметров, необходимая для прогноза - примененные методы лечения. Эти параметры неизвестны при поступлении, на этот момент их можно только предполагать. Однако при обучении нейросети используются уже пролеченные больные с известным набором терапевтических и хирургических воздействий. Обучив нейросети прогнозировать исходы тромбангиита в зависимости от исходного статуса и проведенного лечения, можно моделировать результат, оставляя неизменными фиксированные параметры и подстраивая предполагаемые методы лечения.
Другой блок ЭС обучается прямому выбору наиболее оптимальных методов лечения (блок " Л "), используя только первый, фиксированный набор параметров (рис. 5.6).
С учетом поставленной задачи были сформированы подгруппы примеров для обучения нейросетей. Для решения подзадач блока " И " примеры были сгруппированы по классам четырьмя способами ( таблица 5.6), для блока " Л " - 11 способами ( таблица 5.7).
Для тестирования обученных нейросетей использовались 35 клинических примеров обследованных и пролеченных больных с известными исходами заболевания. Эти примеры не входили в обучающую выборку. Тест каждого примера проводился следующим образом. Сначала тестировались 4 нейросети, прогнозирующие исходы заболевания, причем в качестве параметров лечения, проведенного в клинике, использовались данные о реально назначенном хирургами лечении. Затем пример тестировался нейросетями, назначающими оптимальный набор методов лечения.
После этого проводился повторный тест нейросетями, прогнозирующими исходы, но теперь в пример подставлялись предполагаемые методы лечения, назначенные нейросетями.
| Подзадача | Классы | Число примеров |
|---|---|---|
| 1. Прогноз динамики ишемии | 1. Уменьшение ишемии 2. Без изменений 3. Усиление ишемии |
85 38 7 |
| 2. Прогноз динамики трофических расстройств | 1. Динамики нет 2. Уменьшение трофических расстройств |
50 80 |
| 3. Прогноз исчезновения болей в покое | 1. Боли остались 2. Боли исчезли |
57 73 |
| 4. Ампутация | 1. Не производилась 2. Производилась |
123 7 |
| Подзадача | Классы | Число примеров |
|---|---|---|
| Прогнозирование возможности успешного лечения ("фильтрующая" нейросеть) | 1. Больные с неблагоприятным исходом после лечения 2. Больные с благоприятным исходом и больные со смоделированным лечением |
24 106 |
| 1. Назначение вазапростана | 1. Не назначать 2. Назначать |
122 8 |
| 2. Плазмоферез, иммунопротекторы | 1. Не назначать 2. Назначать |
111 19 |
| 3. Пульстерапия | 1. Не проводить 2. Проводить |
126 4 |
| 4. Симпатэктомия | 1. Не проводить 2. Односторонняя 3. Двухсторонняя |
104 21 5 |
| 5. Деструкция надпочечников | 1. Не проводить 2. Односторонняя 3. Двухсторонняя |
84 25 21 |
| 6. Эмболизация надпочечников | 1. Не проводить 2. Односторонняя 3. Двухсторонняя |
82 41 7 |
| 7. Компактотомия или РОТ | 1. Не проводить 2. Проводить |
120 10 |
| 8. Ревизия | 1. Не проводить 2. Проводить |
127 3 |
| 9. Ампутация | 1. Не проводить 2. Проводить |
125 5 |
| 10. Реконструктивная операция | 1. Не проводить 2. Проводить |
126 4 |
| 11. Некрэктомия | 1. Не проводить 2. Проводить |
125 5 |
Рассмотрим результаты первого теста. Нейросеть, прогнозирующая динамику ишемии, сделала правильное заключение в 29 случаях из 35 ( 82,9% ). Регресс трофических расстройств прогнозировался правильно в 14 из 17 случаях имеющихся трофических расстройств (только у 17 больных имелись трофические расстройства, поэтому в остальных случаях прогноз не имел смысла). Это составило 82,4%. Нейросеть, прогнозирующая динамику болевого синдрома, сделала правильное предсказание в 22 из 25 случаев ( 88% ). Ответы сети, отвечающей за предполагаемую ампутацию, совпали в 33 случаях из 35 ( 94,3% ).
Всего в тестирующей выборке имелось 9 больных, у которых не совпал хотя бы один прогноз. У остальных пациентов все прогнозы делались 4 нейросетями правильно. Из этих 9 больных 7 были отнесены нейросетью-"фильтром" к категории "трудных".
Интерес представляют два формально неверных результата нейросети, прогнозирующей ампутацию. У данных больных ампутация не была проведена в сроки госпитализации, однако была выполнена в первые 2 месяца после выписки. Нейросеть правильно предсказала отсроченные исходы, поэтому эти два случая нельзя считать явными ошибками.
Рассмотрим результаты теста нейросетей, назначающих лечение больным. У 12 примеров из 25 ( 35 примеров минус признанные "трудными" нейросетью-"фильтром") лечение, назначенное нейросетями, полностью совпало с реально назначенным хирургами, и только в одном случае прогноз исходов оправдался лишь в более поздние сроки. Рассмотрим этот случай.
Больной С., 42 лет, болен в течение 5 лет, поступил с критической ишемией (IV степени). Больному была назначена консервативная терапия и вазапростан. На фоне такой терапии 3 из 4 нейросетей прогнозировали улучшение состояния. Однако на момент выписки эффекта от лечения не наблюдалось. Тем не менее, при дальнейшем наблюдении за больным отмечался регресс ишемии, регресс трофических расстройств и купирование болей в покое.
В остальных случаях наблюдались некоторые расхождения. При этом у 10 больных нейросети назначили другое лечение, которое (по результатам анализа хирургов), можно было действительно назначить данным больным. Исходы, прогнозируемые после такого лечения, были такими же, как и в случае реально назначенных лечебных мероприятий. В 3 примерах лечение, назначенное нейросетями, было похоже на реально назначенное, однако превосходило его по мощности. В этих случаях прогнозировались исходы, гораздо лучшие, чем наблюдавшиеся в реальности.